Sources principales : (INRS, 2004 ), (INRS, 2010
), (INRS, 2010 ) et (CRCM, 2001
) et (CRCM, 2001 )
)
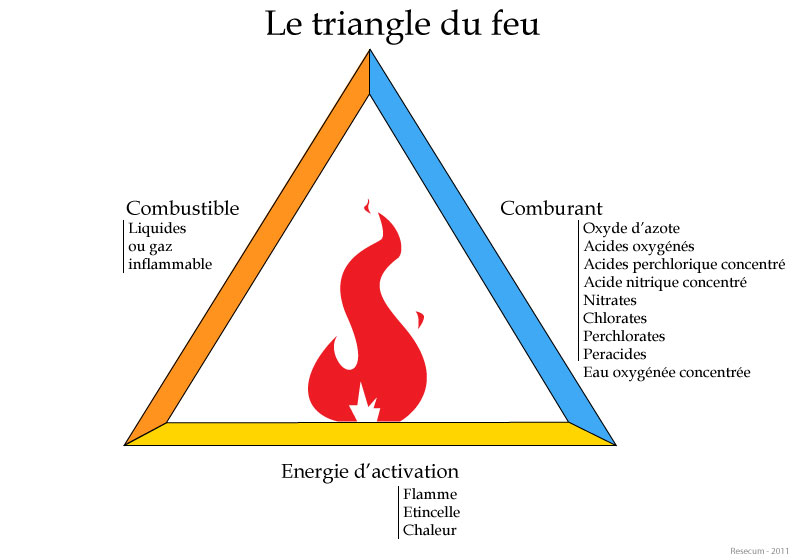
Un incendie est une réaction chimique de combustion qui se développe généralement de façon désordonnée et sans que l’on puisse la contrôler. La combinaison d’un corps combustible avec un comburant en présence d’une énergie d’activation entraîne une réaction exothermique qui entraînera elle-même des réactions en chaîne. Cette combinaison est représentée par le Triangle du feu.
 ), (INRS, 2010
), (INRS, 2010 ) et (CRCM, 2001
) et (CRCM, 2001 )
)Un incendie est une réaction chimique de combustion qui se développe généralement de façon désordonnée et sans que l’on puisse la contrôler. La combinaison d’un corps combustible avec un comburant en présence d’une énergie d’activation entraîne une réaction exothermique qui entraînera elle-même des réactions en chaîne. Cette combinaison est représentée par le Triangle du feu.
Figure 46: Triangle du feu
Complément
Le triangle du feu est aussi expliqué par la vidéo suivante :
http://www.youtube.com/watch?v=hAR2Dulc4kM
Si on supprime l’un des trois éléments cela entraîne l’extinction immédiate du feu.
Source d'activation :
C'est une source d'inflammation efficace qui transmet suffisamment d'énergie au mélange inflammable, pour provoquer une combustion se propageant spontanément :
Source d'activation :
C'est une source d'inflammation efficace qui transmet suffisamment d'énergie au mélange inflammable, pour provoquer une combustion se propageant spontanément :
Tableau 13: Exemples de sources d'activation

Combustible :
C'est un corps qui a la particularité de brûler, composé de Carbone et d’Hydrogène. Il joue le rôle de réducteur.
Les paramètres physico-chimiques permettant d’évaluer le risque d’inflammation sont :
Paramètres de diffusion : Pression de vapeur Pv ou Tension de vapeur :
Un liquide enfermé dans un récipient est toujours en présence de sa vapeur. On entend par pression de vapeur, la pression à laquelle la phase gazeuse d’une substance est en équilibre avec sa phase liquide ou solide.
Elle est mesurée par rapport à la pression atmosphérique standard de 1 atm (soit 760 mm Hg ou 101,53 kPa).
C'est un corps qui a la particularité de brûler, composé de Carbone et d’Hydrogène. Il joue le rôle de réducteur.
Les paramètres physico-chimiques permettant d’évaluer le risque d’inflammation sont :
Paramètres de diffusion : Pression de vapeur Pv ou Tension de vapeur :
Un liquide enfermé dans un récipient est toujours en présence de sa vapeur. On entend par pression de vapeur, la pression à laquelle la phase gazeuse d’une substance est en équilibre avec sa phase liquide ou solide.
Elle est mesurée par rapport à la pression atmosphérique standard de 1 atm (soit 760 mm Hg ou 101,53 kPa).

Elle est mesurée par rapport à la pression atmosphérique standard de 1 atm (soit 760 mm Hg ou 101,53 kPa).
Exemples de quelques Pression de vapeur :
Exemples de quelques Pression de vapeur :

Crédits
Source : http://www.tc.gc.ca/fra/canutec/articles-vapeur-437.htm
Ce paramètre a une influence directe sur la volatilité d’un produit. Plus la pression de vapeur est élevée, plus la substance d’évaporera facilement.
Volatilité (indice d'évaporation)
Il caractérise la facilité d'évaporation d'un produit par rapport à l'éther éthylique :
Volatilité (indice d'évaporation)
Il caractérise la facilité d'évaporation d'un produit par rapport à l'éther éthylique :
Figure 47: définition de la volatilité
Remarque
La volatilité d’un liquide ne traduit pas forcement de son caractère inflammable.
Exemple du dichlorométhane CH2Cl2. Ce solvant est extrêmement volatile mais ne possède pas de point éclair et est donc non inflammable. D’où ses nombreuses applications dans l’industrie.
Exemple du dichlorométhane CH2Cl2. Ce solvant est extrêmement volatile mais ne possède pas de point éclair et est donc non inflammable. D’où ses nombreuses applications dans l’industrie.
Tableau 14: Volatilité de certain composé chimique.

Le tableau ci-dessus présente la volatilité de certains composés organiques. L’acétone et le benzène ont des indices de volatilité plus faibles que le méthanol et l’isopropanol. C'est-à-dire qu’ils s’évaporeront plus rapidement. La présence de fonction alcool dans une molécule implique la possibilité de former des liaisons hydrogène avec d’autres molécules. Cette propriété explique donc la difficulté d’évaporation de ce type de molécules.
Densité de vapeur
Elle se caractérise par l'équation suivante :
Densité de vapeur
Elle se caractérise par l'équation suivante :
Ce paramètre donne une indication sur le poids de la vapeur d’une substance par rapport à celui de l’air (densité air = 1).
Si la densité de vapeur est supérieure à 1, les vapeurs de gaz auront tendance à se maintenir au niveau du sol. Dans le cas où la densité est proche de 1, les vapeurs se mélangeront facilement à l’air.
Si la densité de vapeur est supérieure à 1, les vapeurs de gaz auront tendance à se maintenir au niveau du sol. Dans le cas où la densité est proche de 1, les vapeurs se mélangeront facilement à l’air.

Paramètres d’inflammabilité :
Les Limites Inférieure et Supérieure d’Inflammabilité (LII et LSI), Domaine d'inflammabilité :
LII (Borne basse) : Concentration minimale d’un gaz (ou d’une vapeur) inflammable dans l’air, à partir de laquelle existe le risque d’explosion.
LSI (Borne haute) : Concentration maximale d’un gaz (ou d’une vapeur) inflammable dans l’air, à partir de laquelle le risque d’explosion n’existe plus momentanément.
Les Limites Inférieure et Supérieure d’Inflammabilité (LII et LSI), Domaine d'inflammabilité :
LII (Borne basse) : Concentration minimale d’un gaz (ou d’une vapeur) inflammable dans l’air, à partir de laquelle existe le risque d’explosion.
LSI (Borne haute) : Concentration maximale d’un gaz (ou d’une vapeur) inflammable dans l’air, à partir de laquelle le risque d’explosion n’existe plus momentanément.
Tableau 15: Exemple de LII et LSI

Figure 48: Domaine d'inflammabilité du propane

Figure 49: Domaine d'inflammabilité du dihydrogène

Tableau 16: Interprétation des 3 zones

Le point d’éclair (Flash point) :
Les vapeurs, dans leur domaine d'inflammabilité, peuvent s'enflammer quand elles atteignent une température donnée : le point éclair. C'est la température minimale à laquelle un combustible commence à émettre des vapeurs susceptibles de former avec l'air un mélange dont l'inflammation se produit au contact d'une petite flamme (amorce). Plus la température est élevée au-dessus du point éclair, plus la combustion est facilitée. Plus le point éclair est bas, plus le liquide est inflammable et donc dangereux !
Les vapeurs, dans leur domaine d'inflammabilité, peuvent s'enflammer quand elles atteignent une température donnée : le point éclair. C'est la température minimale à laquelle un combustible commence à émettre des vapeurs susceptibles de former avec l'air un mélange dont l'inflammation se produit au contact d'une petite flamme (amorce). Plus la température est élevée au-dessus du point éclair, plus la combustion est facilitée. Plus le point éclair est bas, plus le liquide est inflammable et donc dangereux !
Tableau 17: Exemple de point éclair pour quelques produits

Figure 50: Classification des produits inflammables selon l'ancienne et la nouvelle réglementation

La température d’auto-inflammation (auto-ignition)
Température minimale à laquelle un produit amorce spontanément sa combustion sans l’intervention d’une source d’ignition extérieure (flamme ou étincelle).
Température minimale à laquelle un produit amorce spontanément sa combustion sans l’intervention d’une source d’ignition extérieure (flamme ou étincelle).
Tableau 18: Exemple de température d'auto inflammation pour quelques produits

Point de flamme
La température de point de flamme dépasse souvent de quelques degrés celle du point éclair. A cette température, la flamme peut se maintenir et se propager.
Comburant
C'est un corps simple, qui en présence d’un combustible, permet, puis entretien la combustion. L'oxygène reste le plus répandu. Il joue le rôle d'oxydant.
La température de point de flamme dépasse souvent de quelques degrés celle du point éclair. A cette température, la flamme peut se maintenir et se propager.
Comburant
C'est un corps simple, qui en présence d’un combustible, permet, puis entretien la combustion. L'oxygène reste le plus répandu. Il joue le rôle d'oxydant.
Tableau 19:Exemples de comburants

Annexe :
Instabilité des molécules