2.6.1 Les différentes techniques
Plusieurs techniques de phytoremédiation existent (Figure 020 d'après Pilon-Smits, 2005[1])
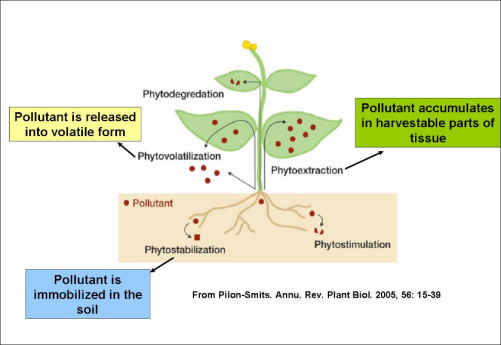
Phytostabilisation ou végétalisation : cette technique consiste à réduire la dispersion des polluants vers les autres compartiments de l'environnement, notamment les nappes et l'atmosphère par limitation de l'érosion du sol par l'eau, le vent ou par entraînement direct. Elle s'adresse en particulier aux sols très pollués où les végétaux habituels ne poussent plus d'où l'utilité de les couvrir avec des plantes tolérantes au polluant.
Phytovolatilisation : cette technique consiste en l'extraction par le végétal de polluants organiques ou inorganiques et relargage atmosphérique par évapotranspiration (Ex : trichloréthylène et peuplier ; méthyl-mercure et tabac). Le polluant (rejeté transformé ou non) peut aussi être exsudé sous forme liquide par les stomates. Alors que dans le sol, les polluants sont récalcitrants à la dégradation, une fois volatilisés, ils subissent une oxydation par les radicaux OH- produits en grande quantité dans les cycles photochimiques. Les meilleurs résultats sont obtenus avec des espèces à forte évapo-transpiration (1-6 m/h en moyenne, jusqu'à 100 m/h).
Rhizodégradation : il s'agit de la dégradation des polluants par les protéines et les enzymes des racines (processus internes) et par l'activité microbienne associée (processus externes) des microorganismes de la rhizosphère (portion de sol sous l'influence de l'activité racinaire de la plante). Les polluants sont minéralisés complètement ou non et peuvent servir de source de substrat pour les plantes et les microorganismes. En retour, les sucres, alcool, acides... excrétés par les plantes peuvent stimuler l'activité microbienne de la rhizosphère et donc la dégradation des polluants. L'action des microorganismes est le plus souvent prépondérante dans les processus de phytodégradation.
Phytodégradation : Dans ce cas, les polluants ne sont pas dégradés dans la rhizosphère mais dans la plante. Le prélèvement du polluant par la plante dépend de son Kow. Il doit être compris entre 1000 et 3000, ce qui est le cas des BTEX – benzène, toluène, ethylbenzène, xylène – des solvants chlorés, des chaînes courtes aliphatiques. Au-delà de 3000, le polluant est hydrophobe et n'est plus soluble ou se sorbe à la surface des racines. En-dessous de 10, les polluants sont trop polaires, ne se fixent plus suffisamment sur les racines pour être activement transportés.
Les polluants sont intégrés aux tissus de la plante (couplage covalent à la lignine) ou stockés dans les vacuoles ou dégradés plus ou moins complètement par des enzymes (dégradation en molécules plus simples et souvent moins toxiques) : déhalogénases qui coupent les groupements halogénés des solvants chlorés, oxygénases qui oxydent les molécules aliphatiques, nitroréductases qui réduisent les groupements contenant de l'azote du TNT.
Le transport du polluant des racines vers les parties aériennes dépend de la concentration en polluant dans les racines et de la concentration dans le flux de transpiration, en comparaison de la concentration du même polluant dans le sol. Les valeurs de ces 2 facteurs dépendent directement du Kow (maximum entre 1000 et 3000).
L'efficacité de la mobilisation des polluants dépend aussi du sol (texture, structure[2]), de ses propriétés physico-chimiques, de la spéciation du polluant et de la plante elle-même.
Phytoextraction : technique essentiellement employée pour LES POLLUANTS INORGANIQUES de l'eau, des sols, boues et sédiments de manière :
Passive, dans le flux de transpiration jusqu'aux stomates grâce à un phénomène de translocation, et/ou
Active, associée à des protéines de transport présentes dans la paroi des cellules racinaires.
Les plantes utilisent 13 éléments minéraux indispensables à leur activité biologique sous forme dissoutes (N, P, K, Ca, Mg, S, Fe, Cl, Zn, Mn, Cu, B, Mo) et des éléments minéraux non indispensables (Cd, Pb, As...). L'absorption des éléments non essentiels peut concurrencer l'absorption des éléments minéraux essentiels.
Les plantes peuvent accumuler des éléments toxiques dans les vacuoles, ou les immobiliser à la surface des racines. On peut observer la translocation des métaux dans la plante et accumulation dans les racines, tiges, feuilles, fruits.
Les espèces dites hyper accumulatrices représentent seulement 0,2% des angiospermes (soit environ 450 espèces). Le seuil de concentration en ET dans les parties aériennes au-dessus duquel la plante est considérée comme accumulatrice varie selon l'ET (Tableau 010 d'après Sheoran et al. 2009[3]).
Element | Lower limit for hyperaccumulation (mg/kg) | No. of hyperaccumulators | Families of hyperaccumulators |
|---|---|---|---|
Arsenic | 1000 | 5 | Pteridaceae |
Cadmium | 100 | 2 | Brassicaceae, Asteraceae, Chenopodiaceae |
Cobalt | 1000 | 30 | Lamiaceae, Scrophulariaceae |
Copper | 1000 | 34 | Cyperaceae, Lamiaceae, Brassicaceae, Poacea, Scrophulariaaceae |
Golda | 1 | - | Brassicaceae |
Leada | 1000 | 14 | Compositae, Brassicaceae |
Manganese | 10,000 | 11 | Apocynaceae, Cunoniaceae, Proteaceae |
Nikel | 1000 | 320 | Brassicaceae, Cunoniaceae, Flacortiaceae, Violaceae, Euphorbiaceae |
Selenium | 100 | 20 | Fabaceae, Brassicaceae |
Silvera | 1 | - | Brassicaceae |
Thallium | 100 | 1 | Brassicaceae |
Uraniuma | 1000 | - | Brassicaceae |
Zinc | 10,000 | 16 | Brassicaceae, Crassulaceae, Leguminosae |
Lower limit for hyperaccumulation of various metals and number of known hyperaccumulators with their families (Baker et al., 2000 ; Reeves and Baker, 2000 ; Reeves, 2003, 2006).
a For induced hyperaccumulation.
Quelques plantes annuelles/ligneux sont présentées figure 021.

Les ET habituellement hyperaccumulés sont le Cd, Ni, Zn ; As, Se, Cu. Les métaux modérément accumulés regroupent le Co, Fe. Pb, Cr. L'uranium est peu accumulé. En revanche, Pb, U et le Cs s'accumulent dans les plantes lorsqu'ils sont chélatés respectivement à l'EDTA, à l'acide citrique et au nitrate d'ammonium.




